Các loại van tim nhân tạo
Các loại van tim nhân tạo được chia thành 2 nhóm lớn: van cơ học và van sinh học. Mỗi loại van lại có độ bền, nguy cơ tạo huyết khối, và đặc điểm huyết động khác nhau.

Các loại van tim nhân tạo
Các loại van tim nhân tạo được chia thành 2 nhóm lớn: van cơ học và van sinh học. Mỗi loại van lại có độ bền, nguy cơ tạo huyết khối, và đặc điểm huyết động khác nhau.

Đặc điểm của các loại van tim nhân tạo.
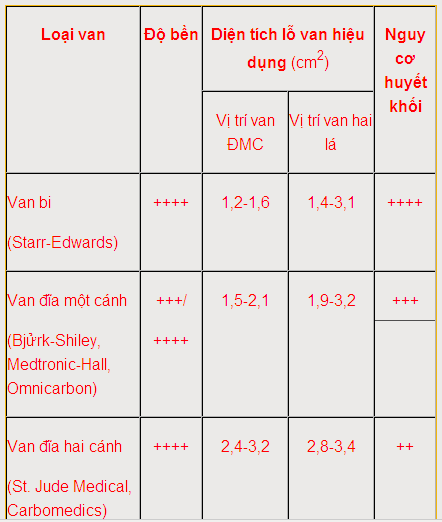


A. Van cơ học
1. Van đĩa một cánh: (van Bjửrk-Shiley, Medtronic-Hall và Omnicarbon) có cấu tạo gồm một vòng van bằng kim loại gắn với một cánh đĩa bằng pyrolytic carbon di động tự do một góc 60-85o xung quanh một trục, tạo thành hai lỗ lớn để máu lưu thông.
2. Van đĩa hai cánh: (van St. Jude Medical, Carbomedics) gồm hai cánh đĩa bán nguyệt di động tự do một góc 75-90o ở hai bên, tạo thành một diện chữ nhật và hai lỗ lớn hai bên cho máu lưu thông khi van mở. Van được thiết kế để có một dòng hở nhỏ trong van nhằm giảm hình thành huyết khối trên đĩa. Hiện là loại được dùng phổ biến do nhiều ưu điểm về huyết động.
3. Van bi (lồng) (van Starr-Edwards): gồm một viên bi bằng silicon di động tự do trong lồng chụp kim loại, máu sẽ đi xung quanh viên bi. Loại này hiện gần như không còn sử dụng do nhiều nhược điểm về huyết động.
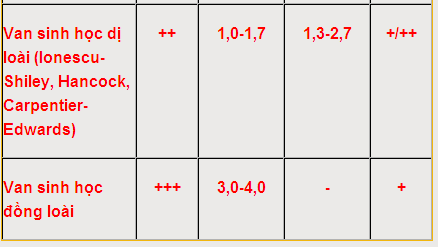
B. Van sinh học: mặc dù rất giống van tự nhiên song về huyết động vẫn chưa phải đã tối ưu do kích thước van bị các thành phần vòng van, phần chống đỡ van làm nhỏ đi.
1. Van dị loài: bằng cách phủ lên một giá đỡ và một vòng van kim loại màng tim bò hoặc van tim lợn đã qua xử lý như van Carpentier-Edwards. Các loại van mới như Hancock II hoặc Medtronic Freestyle, St. Jude-Medical có cải tiến huyết động do cách gắn van trực tiếp với ĐMC hoặc đặt van ngồi trên vòng van...
2. Van đồng loài: chủ yếu ở vị trí van ĐMC bằng cách lấy van từ người hiến tạng, có thể kèm thêm một đoạn ĐMC, bảo quản lạnh trong ngân hàng mô. Việc phát triển còn gặp nhiều khó khăn và hạn chế.
II. Lựa chọn loại van để thay
1. Sửa van:
Cần phải xem xét khả năng van còn sửa được hay không trước khi quyết định thay van, do sửa van có ưu thế hơn hẳn như: bảo tồn được chức năng thất trái vì giữ được các tổ chức dưới van, tỷ lệ tử vong chu phẫu thấp, không cần dùng thuốc chống đông, tỷ lệ sống còn lâu dài tốt. Hiện nay, chủ yếu mới áp dụng rộng rãi các kỹ thuật sửa van hai lá, còn đối với van ĐMC thì khó sửa hơn rất nhiều, chỉ nên làm hạn chế trong một số trường hợp không do thấp tim như van ĐMC hai lá bẩm sinh gây HoC do sa van, van không vôi, không hẹp…
Bảng 17-2. So sánh giữa mổ thay van và sửa van.
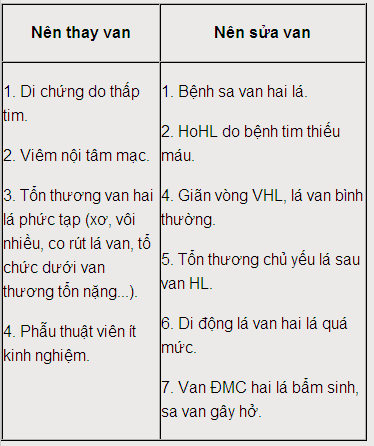
2. Van sinh học dị loài: chỉ định thay cho bệnh nhân không thể dùng thuốc chống đông kéo dài, bệnh nhân tuổi cao (> 70), cũng nên cân nhắc thay van sinh học cho những bệnh nhân nữ còn muốn có thai. Cần chú ý nguy cơ thoái hoá van phải mổ thay van lại (tỷ lệ mổ lại 40% nếu tuổi bệnh nhân 70).
3. Van đồng loài (sinh học): có độ bền cao hơn, chênh áp qua van thấp nhất so với các loại van sinh học khác nhưng sau 20 năm chỉ 10% van hoạt động còn tốt. Van ĐMC đồng loài được lựa chọn cho bệnh nhân tuổi < 50, phụ nữ còn muốn có thai, bệnh nhân không thể dùng thuốc chống đông kéo dài, bệnh nhân cần thay cả van và đoạn ĐMC và đặc biệt là bệnh nhân viêm nội tâm mạc nhiễm khuẩn tại van ĐMC có biến chứng (ápxe, dò...).
4. Van cơ học: chỉ định cho bệnh nhân tuổi < 60 (do độ bền cao, ít cần mổ lại), ở bệnh nhân phải dùng thuốc chống đông (do rối loạn nhịp hoặc đột quỵ). Bệnh nhân cần thay cả van hai lá và động mạch chủ nên thay van cơ học vì van hai lá sinh học nhanh thoái hoá. Do cấu trúc gọn nên bệnh nhân có kích thước thất nhỏ nên thay van cơ học. Quyết định lựa chọn từng loại van cụ thể còn phụ thuộc vào cấu tạo và đặc điểm huyết động từng loại van: van St. Jude Medical và Metronic-Hall được ưa chuộng nhất do ưu thế về huyết động, độ bền cao và tỷ lệ biến chứng thấp...
III. Theo dõi sau mổ thay van
Việc theo dõi sau mổ thay van tim nhân tạo là hết sức cần thiết, gồm theo dõi triệu chứng lâm sàng và xét nghiệm, dù bệnh nhân không có triệu chứng cơ năng. Kết quả siêu âm Doppler tim trong vòng 1-6 tuần ngay sau mổ được dùng làm mốc để theo dõi về sau. Thông thường nên kiểm tra định kỳ siêu âm tim 1 năm một lần hoặc mau hơn nếu có triệu chứng cơ năng, nhất là giai đoạn 5 năm sau mổ trở đi. Tuyên truyền cho bệnh nhân về nguy cơ và sự cần thiết phải điều trị dự phòng viêm nội tâm mạc.
Riêng với bệnh nhân có van cơ học, cần theo dõi định kỳ hiệu quả của thuốc chống đông bằng xét nghiệm tỷ lệ Prothrombin và INR.
1. Dùng thuốc chống đông sau mổ thay van:
a. Đối với van cơ học:
· Ngay sau mổ thay van có rất nhiều cách dùng thuốc chống đông. Dùng sớm quá sẽ làm tăng nguy cơ tràn máu màng tim, ép tim hoặc chảy máu sau mổ. Một số nơi chỉ bắt đầu dùng thuốc chống đông đường uống 3-4 ngày sau mổ thay van. Một số khác dùng Heparin tĩnh mạch liều thấp (để aPTT đạt ngưỡng bình thường cao) ngay từ 6-12 giờ sau mổ, tăng Heparin lên đủ liều sau rút dẫn lưu ngực, bắt đầu uống thuốc chống đông từ 24-48 giờ sau mổ. Dù sao nên xét kỹ nguy cơ huyết khối của từng bệnh nhân và vị trí van (van hai lá cao hơn van ĐMC).
· Về lâu dài: uống thuốc chống đông (thuốc kháng vitamin K) để duy trì giá trị INR trong ngưỡng tác dụng.
Bảng 17-3. Ngưỡng tác dụng chống đông cho các loại van tim nhân tạo.
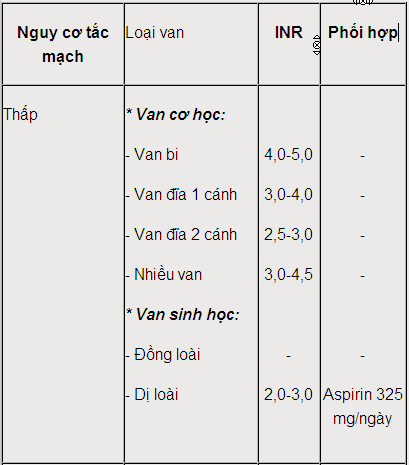

· Dùng thuốc chống đông lâu dài có nguy cơ chảy máu nhẹ (2-4%/năm), chảy máu nặng (1-2%/năm), tử vong 0,2-0,5%/năm. Nguy cơ chảy máu tăng ở tuổi già (5-6% ở bệnh nhân > 70 tuổi). Nguy cơ xảy ra tắc mạch cho dù vẫn dùng thuốc chống đông là 1%/năm.
b. Đối với van sinh học: việc dùng thuốc chống đông sau mổ thay van sinh học còn nhiều bàn cãi. Nguy cơ tắc mạch cao nhất sau mổ và giảm dần trong 3 tháng sau mổ, tỷ lệ huyết khối ở vị trí van hai lá (7%) cao hơn so với vị trí van ĐMC (3%). Vì thế cần dùng thuốc chống đông đường uống sau mổ thay van sinh học trong 3 tháng đầu sau mổ, rồi chuyển sang Aspirin 325 mg/ngày. Những bệnh nhân đã có tiền sử tắc mạch, rung nhĩ, rối loạn chức năng thất trái nên uống thuốc chống đông suốt đời.
2. Điều chỉnh liều chống đông khi làm các thủ thuật không phải tim mạch:
a. Đối với các thủ thuật lớn, mất máu nhiều, nên dừng thuốc chống đông đường uống ít nhất 3 ngày trước khi làm thủ thuật để INR £ 1,6. Cần điều trị gối bằng Heparin tiêm tĩnh mạch ở bệnh nhân có van bi, rung nhĩ, huyết khối nhĩ trái, rối loạn chức năng thất trái nặng, tiền sử tắc mạch.
b. Đối với những thủ thuật nhỏ (như nhổ răng...), nguy cơ chảy máu ít, có thể vẫn duy trì tiếp liều chống đông đang dùng.
c. Sau mổ, dùng lại Heparin ngay khi có thể, sau đó gối tiếp bằng thuốc chống đông đường uống để duy trì lâu dài.
3. Điều chỉnh quá liều chống đông:
a. Liều thuốc chống đông khởi đầu nên là 5 mg Warfarin (tương đương 1 mg Acenocoumaron (SintromÒ) hay 5 mg Fluindione (PreviscanÒ). Phải giảm bớt liều ở người già, người có bệnh gan mật phối hợp hoặc có nguy cơ chảy máu cao.
b. Nếu INR vượt ngưỡng điều trị và < 5,0 thì nên hạ bớt liều điều trị hoặc tạm dừng một ngày và uống với liều hạ thấp hơn.
c. Nếu INR > 5,0 và < 9,0 mà không chảy máu đáng kể, tạm ngừng thuốc chống đông một hoặc hai ngày, theo dõi thường xuyên INR, uống lại thuốc với liều thấp hơn khi INR đã về ngưỡng điều trị hoặc tạm dừng một ngày thuốc, uống 1-2,5 mg vitamin K1 nhất là khi nguy cơ chảy máu cao.
d. Nếu cần nhanh hơn (chẳng hạn cần mổ cấp) thì uống 2-4 mg vitamin K1 (INR sẽ giảm đáng kể sau 24h). Nếu INR vẫn còn cao thì chỉ uống thêm 1-2mg vitamin K1 mà thôi.
e. Nếu INR > 9,0 mà không chảy máu đáng kể, thì dừng ngay thuốc chống đông, phối hợp uống 3-5mg vitamin K1 (INR sẽ giảm đáng kể sau 24-48h), lặp lại nếu cần, theo dõi sát và dùng lại thuốc chống đông với liều thấp khi INR đã nằm trong ngưỡng điều trị.
f. Nếu INR > 20 có kèm chảy máu nặng, dừng ngay thuốc chống đông, truyền tĩnh mạch chậm 10 mg vitamin K1, phối hợp với truyền huyết tương tươi hoặc tủa prothrombin tuỳ trường hợp, có thể lặp lại 12h/lần.
4. Thuốc chống đông và thai nghén: tỷ lệ biến chứng tắc mạch do huyết khối tăng lên khi có thai. Tuy nhiên do tác dụng gây dị tật bẩm sinh, nên ngừng thuốc chống đông đường uống (kháng vitamin K) trong ba tháng đầu sau khi có thai, thay bằng Heparin tiêm dưới da 15.000 đơn vị ´ 2 lần/ngày nhằm duy trì thời gian aPTT gấp 1,5-2,0 lần so với chứng (lấy xét nghiệm sau tiêm 6 giờ) ít nhất cho đến 3 tháng giữa, khi đó có thể quay lại uống thuốc chống đông tiếp cho tới giữa 3 tháng cuối. Đến lúc đó, chuyển lại tiêm dưới da Heparin 5.000 đơn vị ´ 2 lần/ngày cho tới lúc chuyển dạ. Có thể phối hợp với Aspirin liều thấp.
IV. Triệu chứng lâm sàng và xét nghiệm ở bệnh nhân có van tim nhân tạo
A. Triệu chứng lâm sàng: biểu hiện của rối loạn hoạt động van nhân tạo tương đối phức tạp (xem thêm phần biến chứng van nhân tạo).
1. Tiền sử và bệnh sử: nên hỏi kỹ hoặc kiểm tra hồ sơ ra viện về các vấn đề liên quan đến van nhân tạo như: chỉ định thay van; vị trí van nhân tạo; loại và kích thước van; thời gian kể từ khi thay; các biến chứng liên quan đến dùng thuốc chống đông, biến chứng tắc mạch, viêm nội tâm mạc, sốt hoặc thay đổi âm sắc tiếng đập của van.
2. Khám thực thể: để phát hiện các tiếng thổi mới, âm nghẹt hoặc các biểu hiện huyết khối kẹt van. Bản thân van nhân tạo đã làm thay đổi tiếng bình thường do di chuyển cánh van hoặc do thay đổi tính chất của dòng chảy qua van. Các tiếng, âm sắc của van nhân tạo đã che lấp những tiếng tim bình thường. Mặt khác những âm sắc này có thể không hề thay đổi cho dù đã rối loạn nặng hoạt động của van. Tuy nhiên nếu đã quen với các tiếng van tim nhân tạo thì nghe tim cũng giúp ích được nhiều cho việc chẩn đoán bệnh lý của van nhân tạo trước khi sử dụng các biện pháp chẩn đoán hình ảnh khác.
B. Các xét nghiệm chẩn đoán: xác định rối loạn hoạt động van nhân tạo chủ yếu dựa trên hình ảnh siêu âm Doppler tim, cho phép đánh giá sớm trước khi biểu lộ ra triệu chứng lâm sàng.
1. Siêu âm Doppler tim: cần đánh giá đầy đủ cấu trúc của van, các thành phần của bộ máy van nhân tạo, chênh áp trung bình và tối đa qua van, dòng hở trong van hoặc quanh van. Siêu âm tim qua thực quản được chỉ định cho những trường hợp nghi ngờ hoặc đã có triệu chứng của viêm nội tâm mạc nhiễm khuẩn. Nói chung, kỹ thuật làm siêu âm không khác gì so với các van tự nhiên, song khó hơn do van nhân tạo gây ra các bóng cản âm.
a. Rối loạn hoạt động của van thường biểu hiện ở chỗ các lá van đóng không kín (do huyết khối, do vôi hoá van sinh học hay do nội mạc tăng sinh quá mức), di động quá mức vòng van (biểu hiện của long van, có thể kèm theo các tổn thương xung quanh như ápxe, dò, giả phình cạnh vòng van gây ra do viêm nội tâm mạc van nhân tạo).
b. Siêu âm Doppler màu cung cấp các kết quả đo đạc gián tiếp nhưng đáng tin cậy về hoạt động của van nhân tạo: như chênh áp qua van (từ đó ước tính diện tích lỗ van hiệu dụng), dòng hở trong van hoặc quanh van, cơ chế gây hở van...
c. Đánh giá hở van nhân tạo:
· Đối với van cơ học, dòng hở được coi là sinh lý nếu diện tích hở < 2 cm2 và độ dài dòng hở < 2,5 cm ở vị trí van hai lá hoặc diện tích hở < 1 cm2 và độ dài dòng hở < 1,5 cm ở vị trí van động mạch chủ. Phần lớn các van sinh học đều có dòng hở nhẹ (sinh lý) ngay sau khi thay van.
· Dòng hở van bệnh lý thường rộng và dài hơn nhiều, có thể có nhiều dòng hở, thường liên quan đến hiện tượng vôi, sẹo hoá vòng van, hư hại cấu trúc van, áp xe vòng van, tổ chức lân cận... Siêu âm tim qua thực quản sẽ giúp lượng giá khá chính xác mức độ hở van đặc biệt là trong trường hợp hở chân (quanh) van.
· HoHL được coi là nặng khi vận tốc tối đa đầu tâm trương ³ 2,5 m/giây hoặc PHT dòng chảy qua van hai lá £ 150 miligiây.
· HoC được coi là nặng khi PHT dòng chảy qua van ĐMC £ 250 miligiây hoặc có dòng chảy ngược trong động mạch chủ xuống.
d. Đánh giá hẹp van nhân tạo:
· Chênh áp qua van:
(a) Van nhân tạo nào cũng ít nhiều tạo ra một chênh áp qua van. Chênh áp qua van tính trên siêu âm Doppler liên tục sau mổ vài tuần được coi là giá trị tham chiếu để theo dõi sau này.
(b) Chênh áp qua van cao không những do hẹp van mà còn do tình trạng tăng cung lượng, thiếu máu, nhịp nhanh, hở van nhân tạo nhiều hoặc hiện tượng “phục hồi áp lực” (rất hay gặp ở van cơ học hai cánh ở vị trí van ĐMC, có hiện tượng áp lực tăng thứ phát sau khi dòng chảy đi qua lỗ hẹp, làm tăng chênh áp thực sự qua van lên khoảng 1/3 song nếu đã hẹp van, thì hiện tượng này giảm đi).
· Diện tích lỗ van: Phương trình liên tục cho phép ước tính diện tích lỗ van chức năng:
Diện tíchvan ĐMC = (Đường kính vòng van)2 ´ 0,785 ´ VTIĐRTT/VTIvan ĐMC
Diện tíchvan HL = (Đường kính ĐRTT)2 ´ 0,785 ´ VTIĐRTT / VTIvan HL
Trong đó ĐRTT là đường ra thất trái, VTI là tích phân vận tốc theo thời gian dòng chảy tính bằng siêu âm Doppler liên tục.
· Thời gian bán giảm áp lực (PHT): có ích để đánh giá diện tích lỗ van hai lá nhân tạo (=220/PHT), đồng thời cho phép phân biệt nguyên nhân gây tăng VTI dòng chảy qua van hai lá (nếu PHT cũng tăng, nguyên nhân là hẹp van), nếu PHT không kéo dài, thì nguyên nhân chỉ là tăng dòng chảy qua van. Tuy nhiên diện tích lỗ van tính theo PHT đôi khi sẽ lớn hơn giá trị thực.
· Chỉ số tỷ suất giữa vận tốc dòng chảy ở đường ra thất trái và van ĐMC nhân tạo cho phép đánh giá có hẹp van hay không nhất là khi không biết rõ đường kính vòng van. Chỉ số VĐRTT/Vvan ĐMC này càng lớn thì diện tích lỗ van càng lớn, nếu < 0,23 thì hẹp van đáng kể.
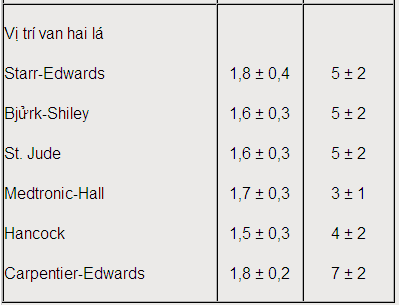
Bảng 17-4. Một số thông số bình thường của các loại van tim nhân tạo khi đo bằng siêu âm Doppler tim.
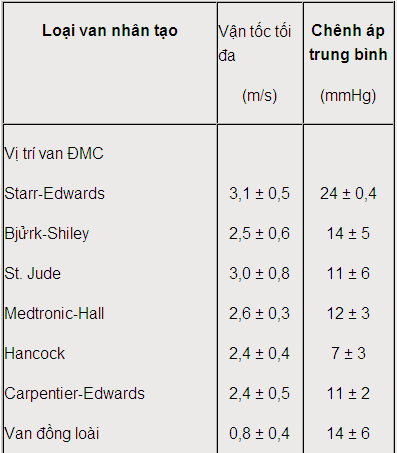
2. Soi dưới màn tăng sáng: chỉ có ích trong trường hợp các van cơ học. Nếu chỉnh để chùm tia X đi song song với mặt phẳng của van thì hình ảnh đóng mở các cánh van là rõ nhất. Di động cánh van giảm là dấu hiệu của tắc nghẽn van, ngược lại di động vòng van quá lớn (> 7o đối với van ĐMC và > 11o đối với van hai lá) là dấu hiệu của long (hỏng) van một phần.
3. Thông tim trái vào thất trái có thể tiến hành an toàn ở bệnh nhân có van ĐMC sinh học để đo chênh áp qua van, nhưng đối với van ĐMC cơ học (chống chỉ định đưa ống thông qua) thì phải xuyên vách liên nhĩ rồi đưa ống thông xuống thất trái. Đối với van hai lá cũng phải làm tương tự để đo được chênh áp. Chống chỉ định đưa ống thông qua các van cơ học (lồng bi, lồng đĩa, một hay hai cánh).
4. Chụp cộng hưởng từ (MRI): cho phép xác định hở van, rò quanh van, hoặc ápxe vòng van nếu có chống chỉ định làm siêu âm qua thực quản. Chụp cắt lớp theo tỷ trọng (CT) không có giá trị trong việc đánh giá hoạt động van nhân tạo.
C. Rối loạn hoạt động của van nhân tạo và các biến chứng liên quan
1. Rung nhĩ: có tới một nửa số bệnh nhân thay/sửa van xuất hiện rung nhĩ sau mổ. Điều trị loại rung nhĩ này không khác gì so với điều trị rung nhĩ nói chung.
a. Đối với bệnh nhân chưa có tiền sử rung nhĩ thì thường tự trở về nhịp xoang. Nhưng nếu rung nhĩ dai dẳng, kéo dài > 24 giờ, thì cần xem xét điều trị thuốc chống đông và chuyển nhịp bằng thuốc chống loạn nhịp hoặc sốc điện.
b. Điều trị dự phòng trước mổ bằng thuốc chẹn b giao cảm hoặc Amiodarone có tác dụng rõ rệt làm giảm tỷ lệ rung nhĩ sau mổ tim.
2. Rối loạn dẫn truyền: bloc nhĩ thất phải đặt máy tạo nhịp chiếm khoảng 2-3% sau mổ thay van và khoảng 8% sau mổ lại van. Nguyên nhân thường do sang chấn bó His trong mổ hoặc phù nề tổ chức quanh van sau mổ. Các yếu tố như vôi hoá vòng van ĐMC hoặc hai lá, rối loạn dẫn truyền trước mổ, tuổi cao, viêm nội tâm mạc nhiễm khuẩn, phẫu thuật van ba lá làm tăng nguy cơ rối loạn dẫn truyền sau mổ, có thể dẫn tới phải đặt máy tạo nhịp vĩnh viễn.
3. Viêm nội tâm mạc nhiễm khuẩn (VNTMNK): Tỷ lệ VNTMNK ở bệnh nhân thay van nhân tạo xấp xỉ 3-6%, với đặc điểm cục sùi rất lớn (do vi khuẩn gây bệnh cư trú trên van, nên có thể tránh khỏi các cơ chế bảo vệ của cơ thể). Thường chia làm 2 loại:
a. VNTMNK trên van tim nhân tạo sớm: trong vòng 60 ngày sau mổ: chủ yếu do tụ cầu da (S. epidermidis), diễn biến rất nặng, dễ dàng đưa đến tử vong (20-70%).
b. VNTMNK trên van tim nhân tạo muộn: thường xảy ra ở bệnh nhân có nhiều van nhân tạo hoặc ở vị trí van ĐMC. Lâm sàng nói chung giống VNTMNK trên van tự nhiên. Tác nhân hay gặp nhất là liên cầu, sau đó là vi khuẩn Gram âm, tụ cầu ruột và S. epidermis.
c. Chẩn đoán xác định dựa vào siêu âm tim qua thực quản do độ nhậy và đặc hiệu cao (90-95%); đồng thời xác định các biến chứng khác như áp xe vòng van, long van, rò van..; cũng như dùng siêu âm để theo dõi hiệu quả điều trị.
d. Điều trị: nếu chỉ dùng kháng sinh đơn thuần, tỷ lệ tử vong lên tới 61% (so với 38% nếu thay van) do khả năng thành công rất thấp (cắt sốt) với các tác nhân như tụ cầu, vi khuẩn gram âm hoặc nấm, còn với liên cầu đáp ứng cũng chỉ khoảng 50%.
e. Bệnh nhân VNTMNK van tim nhân tạo vẫn nên dùng thuốc chống đông. Nếu không dùng thuốc chống đông, nguy cơ đột quỵ khi có thêm VNTMNK tăng lên tới 50% trong khi nếu dùng chống đông thì tỷ lệ tắc mạch chỉ là 10%. Hiện chưa có kết luận chắc chắn nào về việc tăng nguy cơ xuất huyết não ở bệnh nhân VNTMNK van nhân tạo có dùng thuốc chống đông.
f. Chỉ định mổ thay lại van tim nhân tạo khi:
· Tiếp tục nhiễm khuẩn huyết dù đã điều trị kháng sinh rất tích cực.
· VNTMNK ăn thủng các tổ chức xung quanh hoặc tạo đường dò.
· Cục tắc gây nghẽn mạch tái phát.
· VNTMNK do nấm.
· Long van hoặc tắc van nhân tạo.
· Tắc nghẽn đường dẫn truyền mới hoặc rối loạn dẫn truyền nặng hơn.
· Suy tim ứ huyết tiến triển hoặc rối loạn huyết động nặng.
4. Tan máu: gặp ở rất nhiều bệnh nhân thay van cơ học nhưng hiếm khi biểu hiện ra triệu chứng lâm sàng.
a. Tỷ lệ thiếu máu do tan máu gặp ở 6-15% bệnh nhân thay van bi, song hiếm gặp hơn ở van đĩa hoặc van sinh học. Thiếu máu do tan máu thường gặp ở bệnh nhân có nhiều van nhân tạo, van nhân tạo cỡ nhỏ, hở quanh van và VNTMNK trên van nhân tạo... với cơ chế liên quan đến dòng máu xoáy có áp lực cao đập vào các tổ chức kim loại.
b. Chẩn đoán xác định khi có tăng men LDH, tăng hồng cầu lưới, tăng bilirubin gián tiếp, haptoglobin niệu và xuất hiện các mảnh vỡ hồng cầu trên lam máu. Siêu âm tim thường phát hiện thấy có hiện tượng va đập của dòng máu có tốc độ cao (dòng hở lệch tâm hoặc quanh van) va vào các tổ chức van nhân tạo.
c. Thiếu máu tan máu nhẹ có thể điều trị bổ sung với sắt, acid folic và truyền máu. Dùng thuốc chẹn bêta giao cảm và kiểm soát tốt huyết áp có thể làm giảm mức độ nặng của tán huyết.
d. Mổ lại để sửa hở quanh van hoặc thay van được chỉ định cho những bệnh nhân thiếu máu tan máu nặng cần phải truyền máu nhiều lần hoặc có suy tim ứ huyết.
5. Huyết khối: tỷ lệ huyết khối tại van chiếm khoảng 0,2-1,8%/năm, hay gặp nhất ở vị trí van ba lá, sau đó là vị trí van hai lá và cuối cùng là vị trí van ĐMC.
a. Nên nghĩ tới huyết khối kẹt van ở bệnh nhân có triệu chứng khởi phát đột ngột, có tiền sử tắc mạch hoặc dùng thuốc chống đông không đủ. Siêu âm tim qua thực quản là biện pháp thường dùng nhất để chẩn đoán huyết khối tại van, tuy có thể phát hiện hình ảnh hạn chế vận động của van nhân tạo khi soi trên màn chiếu Xquang. Hình ảnh trên siêu âm gợi ý huyết khối là một khối di động, mật độ mềm, không đồng đều.
b. Điều trị: cách thức xử trí phụ thuộc vào vị trí huyết khối của van chứ không phụ thuộc vào loại van hay thời gian giả định hình thành huyết khối.
· Trước khi điều trị:
(a) Heparin được dùng sớm ngay từ khi nghĩ tới và khảo sát bệnh. Tiếp tục dùng chống đông đường uống (thuốc kháng vitamine K) trừ phi có chỉ định mổ lại rõ.
(b) Siêu âm tim qua thực quản hoặc ít nhất là soi dưới màn tăng sáng nên làm trong vòng 24 giờ kể từ khi khởi phát và lặp lại thường xuyên nếu còn huyết khối.
c. Điều trị nội khoa:
· Chỉ định dùng thuốc tiêu sợi huyết cho huyết khối van nhân tạo ở tim phải do hậu quả ít nghiêm trọng nếu huyết khối bắn đi xa khi so với bên tim trái. Tỷ lệ thành công lên tới 82%, tỷ lệ biến chứng tắc mạch khoảng 12% và biến chứng chảy máu nặng khoảng 5%.
· Các thuốc hay dùng nhất là: Streptokinase (250.000 đơn vị tiêm trực tiếp tĩnh mạch/30 phút, sau đó truyền tĩnh mạch 100.000 đơn vị/giờ) hoặc Urokinase (4.400 đơn vị/kg/giờ). Thời gian dùng thuốc tiêu sợi huyết thường từ 2 đến 120 giờ, song nên dừng nếu không cải thiện về huyết động sau 24 đến 72 giờ.
· Sau khi dùng thuốc tiêu sợi huyết thành công, cần theo dõi sát hiệu quả điều trị chống đông đường uống cũng như siêu âm Doppler tim lại nhiều lần.
· Chống đông bằng Heparin và Wafarin nói chung được khuyên dùng cho các huyết khối nhỏ (£ 5mm): sử dụng Heparin tiêm tĩnh mạch, sau đó tiêm dưới da 17.000 đơn vị 2 lần/ngày kết hợp uống thuốc kháng vitamin K (duy trì INR từ 2,5-3,5) trong vòng 3 tháng.
d. Phẫu thuật: tỷ lệ tử vong quanh phẫu thuật thấp nhất cũng là 5% vì thế cần cân nhắc nguy cơ của từng bệnh nhân so với khả năng và điều kiện của từng trung tâm. Chỉ định thay van và lấy bỏ huyết khối cho trường hợp huyết khối van nhân tạo tim trái trừ phi huyết khối nhỏ hoặc không thể mổ do nguy cơ phẫu thuật quá cao. Cũng chỉ định mổ nếu điều trị tiêu huyết khối không thành công, mổ sau khi ngừng truyền thuốc 24 giờ.
6. Hỏng hóc cơ học: bong vòng van nhân tạo có thể gặp ngay trong giai đoạn sớm sau phẫu thuật do kỹ thuật mổ kém, vòng van quá vôi hoá, bệnh nhân dùng steroid lâu dài, mô van quá mủn (đặc biệt nếu mổ lại) hoặc nhiễm trùng. Hiện tượng bong van cũng có thể xảy ra muộn do nhiễm trùng. Hình ảnh van đung đưa (lắc lư) trên siêu âm tim hay khi soi dưới màn tăng sáng là một chỉ định mổ lại cấp cứu.
7. Mất tương xứng giữa kích thước van nhân tạo so với bệnh nhân:
a. Tất cả các loại van nhân tạo trừ van tự thân ĐMC (không có vòng kim loại) đều có diện tích lỗ van hiệu dụng thấp hơn hẳn do với van tự nhiên. Vì thế luôn luôn có hiện tượng chênh áp qua van nhân tạo và hẹp van tương đối. Nếu thay vào một van nhân tạo có đường kính quá nhỏ thì sẽ gây ra tình trạng giảm đáng kể cung lượng tim, gây ra các triệu chứng lâm sàng. Hiện tượng này hay gặp nhất khi thay van động mạch chủ ở bệnh nhân hẹp van động mạch chủ.
b. Vì vậy, nếu bệnh nhân có vòng van nhỏ, nên dùng van đồng loại hoặc van đĩa ở vị trí van ĐMC do các ưu thế về huyết động. Van ĐMC nhân tạo có đường kính £ 21mm cũng không nên thay cho bệnh nhân cao lớn hoặc hoạt động thể lực nhiều. Nguyên lý chung là nên cố gắng thay van bằng một van nhân tạo có đường kính lớn hơn, nếu cần thì phối hợp với tạo hình (mở rộng) vòng van.
8. Pannus (hiện tượng tăng sinh nội mạc quá mức phủ trùm lên van): thường phối hợp với huyết khối để gây tắc van (tỷ lệ có thể tới 5% với van cơ học). Cơ chế hình thành pannus còn chưa rõ, có thể liên quan với hiện tượng tăng sinh nguyên bào sợi do phản ứng miễn dịch với dị vật (là van nhân tạo) hoặc phối hợp với các tác nhân như dùng thuốc chống đông không đủ liều, viêm nội tâm mạc nhiễm khuẩn, tác động của dòng máu xoáy qua van hai lá... Nói chung, phải làm siêu âm tim qua thực quản để xác định và khảo sát căn nguyên gây tắc van nhân tạo.
9. Đột quỵ do cục máu đông ở bệnh nhân có van tim nhân tạo:
a. Nguy cơ đột quỵ tái phát khoảng 1%/ngày trong 2 tuần đầu. Nếu chụp phim CT trong vòng 24 và 48 giờ mà không có chảy máu não hoặc nhũn não diện lớn thì nên dùng Heparin đường tĩnh mạch. Duy trì uống thuốc chống đông sẽ làm giảm nguy cơ tái phát đột quỵ xuống một phần ba song lại tăng từ 8-24% nguy cơ chuyển dạng nhũn não thành xuất huyết não nhất là trong vòng 48 giờ đầu tiên. Bổ sung Aspirin hoặc Clopidogrel nếu tái phát đột quỵ dù đã dùng đủ liều thuốc chống đông.
b. Với bệnh nhân có ổ nhũn não lớn, nên tạm dừng thuốc chống đông trong vòng 5-7 ngày đồng thời cũng nên ngừng thuốc chống đông 1-2 tuần nếu có chuyển dạng nhũn não thành xuất huyết.
Tài liệu tham khảo
1. Acar J, Iung B, Boissel JP, et al. Multicenter randomized comparison of low-dose versus standard-dose anticoagulation in patients with mechanical prosthetic heart valves. Circulation 1996;94:2107-2112.
2. Akins CW. Results with mechanical cardiac valvular prosthesis. Ann Thorac Surg 1995;60:1836-1844.
3. Cannegieter SC, Rosendaal FR, Wintzen AR, et al. Optimal oral anticoagulant therapy in patients with mechanical heart valves. N Engl J Med 1995;333:11-17.
4. Davis EA, Greene PS, Cameron DE, et al. Bioprosthetic versus mechanical prosthesis for aortic valve replacement in the elderly. Circulation 1996;94:II-121-125.
5. Garcia MJ. Principles of Imaging. In: Topol EJ. Comprehensive Cardiovascular Medicine. Philadelphia: Lippincott-Raven, 1998: 609-35.
6. Green CE, Glass-Royal M, Bream PR, et al. Cinefluoroscopic evaluation of periprosthetic cardiac valve regurgitation. Am J Radiol 1988;151:455-459.
7. Israel DR, Sharma SK, Fuster V. Anti-thrombotic therapy in prosthetic heart valve replacement. Am Heart J 1994;127:400-411.
8. Jaeger FJ, Trohman RO, Brener S, et al. Permanent pacing following repeat cardiac valve surgery. Am J Cardiol 1994;74:505-507.
9. Lengyal M, Fuster V, Keitni M, et al. Guidelines for management of left-sided prosthetic valve thrombosis: a role for thrombolytic therapy. J Am Coll Cardiol 1997;30:1521-1526.
10. Lin S, Wong J. Prosthetic heart valves. In: Marso SP, Griffin BP, Topol EJ, eds. Manual of Cardiovascular Medicine. Philadelphia: LippincottRaven, 2000.
11. Rahimtoola SH. Prosthetic heart valve performance: long-term follow-up. Curr Probl Cardiol 1992:33ắ406.
12. Shaff IW. Prosthetic Valves. In: Giuliani ER, Oersh BJ, McOoon MD, et al., eds. Mayo Clinic Practice of Cardiology, 3rd ed. St. Louis: Mosby, 1996:1484-1495.
13. Vogel W, Stoll HP, Bay W, et al. Cineradiography for determination of normal and abnormal function in mechanical heart valves. Am J Cardiol 1993;71:225-232.
14. Vongratanasin W, Hillis LD, et al. Prosthetic heart valves. N Engl J Med 1996;335: 407-416.
15. Zabalgoitia M. Echocardiographic assessment of prosthetic heart valves. Curr Probl Cardiol 1992:270-325.