Chẩn đoán và điều trị mảng sườn di động
Chẩn đoán và điều trịÂ mảng sườn di động
Chẩn đoán và điều trịÂ mảng sườn di động
Ổ căn màng phổi sau chấn thương vết thương ngực
click view here
KỸ THUẬT LẤY KHÍ MÁU ĐỘNG MẠCH VÀ PHÂN TÍCH KẾT QUẢ
NGUYÊN LÝ CHUNG
Tổng quan về kỹ thuật
- Phân tích khí máu động mạch (ABG) cần một mẫu máu động mạch để làm xét nghiệm đo pH, áp lực riêng phần CO2 (PaCO2), áp lực riêng phần Oxy (PaO2), bicarbonat (HCO3) và phần trăm bão hòa oxy máu (SaO2) để đánh giá tình trạng hô hấp, chuyển hóa và toan kiềm của bệnh nhân.
- Dựa vào hình dạng đường cong phân ly oxy – hemoglobin cho thấy việc đo lường độ bão hòa oxy máu (SaO2) có thể không phản ánh đúng lượng oxy máu động mạch vì áp lực riêng phần Oxy giảm thấp đáng kể trước khi giảm độ bão hòa oxy máu động mạch. Mặt khác việc xác định độ bão hòa Oxy máu động mạch (SaO2) qua Oximetry có thể chính xác hơn khi tính SaO2 từ khí máu.
- HCO3-Â trong kết quả khí máu động mạch được tính có sự khác biệt so với HCO3-Â được đo trong máu tĩnh mạch.
Dụng cụ
- Dụng cụ lấy mẫu khí máu chuẩn là một syring thủy tinh. Syring được nối với kim, với một kim đủ lớn có thể cho phép máu động mạch tự đẩy lên qua kim và vào trong syring mà không cần phải hút.
- Có rất nhiều loại kít lấy mẫu khí máu động mạch với syring chuyên biệt riêng cho từng bộ kít (xem thêm phần IV.A)
Các lựa chọn khác
- Bằng việc sử dụng các giá trị hiệu chỉnh, kết quả khí máu tĩnh mạch là hữu ích khi không có nghi ngờ về rối loạn oxy hóa máu (trong các trường hợp khí máu động mạch có sự tương đồng tốt với độ bão hòa oxy máu, khi đó không có thay đổi đáng kể nào về quá trình oxy hóa máu).
- Đặt catheter động mạch là cần thiết ở các bệnh nhân cần xét nghiệm khí máu động mạch nhiều lần.
CHỈ ĐỊNH
Chẩn đoán
- Các rối loạn thăng bằng toan kiềm và oxy hóa máu có thể nhanh chóng dẫn đến các rối loạn nhịp tim nặng, không đáp ứng, thậm chí tử vong và giúp người bác sỹ nhận ra được nguyên nhân của các rối loạn như giảm tưới máu mô, rối loạn chuyển hóa, rối loạn hô hấp.
- Cần làm xét nghiệm khí máu động mạch trong các trường hợp rối loạn ý thức không rõ nguyên nhân, các rối loạn về hô hâp, khẳng định các rối loạn giảm oxy hóa máu hoặc các bất thường HCO3-Â
- Sự khác biệt giữa SaO2Â và PaO2Â trên khí máu động mạch có thể gợi ý chẩn đoán carboxyhemoglobinemia và methemoglobinemia.
- PaO2Â trên khí máu động mạch là cần thiết để tính chênh áp oxy phế nang mao mạch trong việc xác định nguyên nhân toan hô hâp và kiềm hô hấp.
- Các giá trị trong khí máu động mạch là cần thiết để đánh giá tổng lượng oxy máu động mạch (CaO2), oxy phân ly (DO2) và oxy tiêu thụ (VO2).
CHỐNG CHỈ ĐỊNH
Việc chọc kim vào một động mạch được tạo hình nhờ phẫu thuật có thể:
- Gây ra một giả phình động mạch
- Làm mất tính toàn vẹn của mảnh ghép
- Làm lan truyền ổ nhiễm khuẩn.
THỦ THUẬT
Thận trọng
- Nếu sử dụng một syring plastic cần lưu ý một số lỗi sau:
+ PaO2Â cũng như Oxy có thể bị thấp giả tạo do bị lỗi áp suất khi PaO2Â trong mẫu vượt quá 221 mmHg.
+ Syring plastic có tỷ lệ diện tích bề mặt lớn làm thay đổi tính thấm của khí khi so sánh với syring 3 ml. Vì lý do này các bộ kít với kim bướm nối với ống dài không nên sử dụng
+ Sử dụng Syring plastic có thể tạo nhiều bọt khí cũng như khó loại bỏ chúng.
+ Khi dùng Syring plastic phải kéo pittông, điều này có thể hút phải máu tĩnh mạch áp lực thấp dẫn tới phân tích mẫu máu tĩnh mạch.
+ Khi kéo pittông để hút máu, bọt khí có thể bị kéo theo vào mẫu. Nếu bọt khí nhiều có thể làm kết quả PaO2Â và PaCO2Â thấp giả tạo.
- Nếu sử dụng quá nhiều heparin sẽ làm thay đổi nồng độ các khí hòa tan (do trong heparin đã có sẵn PO2Â 150 mm Hg; PCO2Â <0.3 mm Hg ở nhiệt độ phòng). Chỉ có khoảng 4% trường hợp xảy ra lỗi này khi dùng 0.2 ml heparin cho 3 – 5 ml máu. Ngược lại nếu dùng ít heparin có nguy cơ tạo cục máu đông trong mẫu. Nếu dùng heparin tinh thể làm giảm nguy cơ pha loãng nhưng tăng nguy cơ tạo cục máu đông.
- Nếu mẫu máu không được xét nghiệm trong vòng 1 phút hoặc không được làm lạnh ở 2 °C, PO2Â và pH sẽ thấp, PCO2Â tăng là do tăng hô hấp tế bào và tăng tiêu thụ O2Â bởi tế bào bạch cầu và tiểu cầu. Điều này là đáng kể nếu có tăng bạch cầu > 40 × 109/L hoặc tăng tiểu cầu 1,000 × 109/L.
- Các mẫu máu có lẫn máu tĩnh mạch sẽ có kết quả PO2Â thấp.
- Ở một người bình thường nếu nhịn thở trong 35 giây sẽ cho kết quả PaO2Â giảm xuống 50 mm Hg, pH giảm 0.07 và tăng PaCO2Â 10 mm Hg.
Vị trí lấy mẫu
- Vị trí tốt nhất là ở động mạch có hệ thống tuần hoàn bàng hệ tốt để không bị giảm tưới máu trong trường hợp co thắt mạch hoặc có cục máu đông. Vị trí động mạch ở nông sát bề mặt da giúp tiếp cận động mạch dễ dàng và đỡ đau. Động mạch quay là vị trí được ưa thích do hội đủ các yếu tố trên. Động mạch trụ cung cấp đủ tuần hoàn bàng hệ ở khoảng 92% người lớn. Tiến hành test Allen thường quy khi chọc khí máu là điều không cần thiết.
- Nếu không tiếp cận được động mạch quay, động mạch mu chân, động mạch chày sau, động mạch thái dương nông (ở trẻ em), động mạch cánh tay, động mạch đùi có thể được lựa chọn thay thế.
- Động mạch cánh tay, động mạch đùi không được lựa chọn ở các bệnh nhân có rối loạn đông máu vì nguy cơ chảy máu gây chèn ép mạch có thể xảy ra.
- Bất kỳ mạch máu nào đã được can thiệp ngoại khoa đều không nên làm thủ thuật.
Kỹ thuật
- Đánh giá kỹ toàn trạng bệnh nhân.
- Bộc lộ bề mặt động mạch được tiếp cận. Nếu tiếp cận động mạch quay, lật ngửa bàn tay, gấp nhẹ cổ tay, sờ động mạch. Cố định tay của bệnh nhân bằng băng dính ở vị trí này.
- Làm sạch vị trí tiếp cận bằng dung dịch alcohol hoặc dung dịch hỗn hợp chlorhexidine/alcohol.
- Tiêm lidocain 1% trong da tạo nốt sần nhỏ bằng kim 25G tại vị trí dự định sẽ chọc kim catheter.
- Nối kim 22G hoặc một kim lớn hơn với một syring thủy tinh có thể chứa 5 ml máu. Tráng kim và syring bằng dung dịch muối heparin (1000UI/ml) hoặc sử dụng bộ kít khí máu có sẵn.
- Chọc kim vào động mạch tạo một góc 30° so với mặt da dọc theo đường đi của mạch máu để tránh chọc vào màng xương nằm dưới động mạch.
- Khi đã tiếp cận được vào trong lòng động mạch và lấy được máu vào trong syring thủy tinh, lấy khoảng 3 ml máu hoặc số lượng tùy theo khuyến cáo của từng bộ kít khí máu cụ thể.
- Ngay sau khi lấy được mẫu máu, loại bỏ các bọt khí nhỏ để chắc chắn mẫu máu không có bọt khí để đảm bảo độ chính xác cho kết quả. Rút kim ra và đóng nắp syring
- Nếu sử dụng syring thủy tinh cần quay tròn syring trong lòng bàn tay từ 5 – 15 giây để trộn đều heparin với máu.
- Ép lên vị trí chọc kim trong khoảng 5 phút (lâu hơn nếu bệnh nhân có rối loạn đông máu). Nếu lấy khí máu ở động mạch cánh tay có thể ép mạch máu mà không bắt được mạch quay.
- Ngâm syring chứa mẫu máu vào túi nước đá (một số bộ kít khí máu không cần thực hiện bước này). Vận chuyển mẫu máu tới phòng xét nghiệm ngay lập tức để phân tích. Đảm bảo rằng mẫu máu được dán nhãn có thời gian lấy và điều kiện thông khí (FiO2 nếu bệnh nhân không thở máy) cũng như nhiệt độ của bệnh nhân.
ĐÁNH GIÁ SAU THỦ THUẬT
Biến chứng
- Nếu lấy khí máu ở động mạch quay thường ít gặp các biến chứng này. Các biến chứng có thể gặp là:
+ Cường phó giao cảm (hiếm gặp)
+ Đau tại chỗ lấy máu có hoặc không kèm theo nín thở (làm sai lệch kết quả)
+ Tụ máu tại chỗ (tỷ lệ nhỏ < 0,58%)
+ Phình mạch lan rộng (thường do chọc kim nhiều lần)
+ Rối loạn các phản xạ giao cảm (thường do chọc kim nhiều lần)
+ Co thắt mạch
+ Chảy máu không kiểm soát được
+ Tắc mạch với biểu hiện thiếu máu ngoại vi
- Nếu lấy khí máu ở động mạch cánh tay hay động mạch đùi là vị trí khó ép có thể gây chảy máu nhiều khó cầm (đặc biệt ở các bệnh nhân rối loạn đông máu)
Giá trị bình thường và hiệu chỉnh
- pH: 7.35 đến 7.45
- PaCO2: 35 đến 45 mm Hg
- PaO2Â (trong giới hạn bình thường, không hút thuốc lá, bệnh nhân trên 40 tuổi: 108.75 - (0.39 × số tuổi) mm Hg
- Nhiệt độ: theo quy ước nên phân tích mẫu khí máu trong điều kiện 37 °C. Mặc dù không có nghiên cứu nào cho thấy cần phải điều chỉnh kết quả khí máu theo nhiệt độ của bệnh nhân. Tuy nhiên khi mẫu máu trên 39 °C thì cần hiệu chỉnh theo nhiệt độ vì ở nhiệt độ thấp hơn độ hòa tan của O2Â và CO2Â sẽ cao hơn, đỡ toan hơn.
- Khi đo lường điện giải từ mẫu máu động mạch, lithium hoặc các điện giải gắn với heparin cần được điều chỉnh. Muối heparin sẽ làm tăng nồng độ Natri và giảm nồng độ Kali. Các lỗi do hòa loãng cũng xảy ra nếu dùng quá nhiều chống đông.
Tài liệu tham khảo
1. Allen E. Thromboangiitis obliterans: methods of diagnosis of chronic occlusive arterial lesions distal to the wrist, with illustrative cases. Am J Med Sci 1929;178:237.
The original paper describing the classic safety maneuver before arterial puncture
2. Petty T, Bigelow B, Levine B. The simplicity and safety of arterial puncture. JAMA 1966;195:181.
A classic article describing arterial puncture
3. Raffin T. Indications for arterial blood gas analysis. Ann Intern Med 1986;105:390.
A good review of the indications for arterial puncture
4. Robinson KA, Markowitz DH, Irwin RS. Arterial puncture for blood gas analysis. In: Irwin RS, Rippe JM, Lisbon A, et al., eds. Procedures and techniques in intensive care medicine, 6th ed. Philadelphia: Lippincott Williams & Wilkins, 2008: 108.
A more detailed account of the method for arterial puncture
5. Sasse S, Berry R, Nguyen T, et al. Arterial blood gas changes during breath-holding from functional residual capacity. Chest 1996;110:958.
The arterial PO2Â fell by 50 mm Hg on average after 35 seconds of breath holding
6. Schmidt C, Mullert-Plathe O. Stability of PO2, PCO2Â and pH in heparinized whole blood samples: influence of storage temperature with regard to leukocyte count and syringe material. Eur J Clin Chem Clin Biochem 1992;30:767.
Storage at 22 °C results in a significant reduction in PO2Â compared to 4 °C.

Phát đồ kiểm soát thuốc kháng đông trong ngoại khoa
Bộ câu hỏi tốt nghiệp chứng chỉ cho cao học lồng ngực & tim mạch
Â
Â
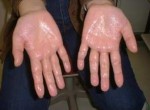
Phẫu thuật nọi soi điều trị chứng ra mồ hôi tay
-20140329000231_150_110.jpg)
Bóng đối xung động mạch chủ
Bóng đối xung động mạch chủ (Intra-Aortic Balloon Pumpe) là một dụng cụ cơ học được sử dụng với mục đích làm tăng lượng oxy tới cơ tim đồng thời làm tăng cung lượng tim. Tăng cung lượng tim sẽ làm tăng dòng máu chảy tới động mạch vành, kết quả là tăng vận chuyển oxy tới tế bào cơ tim. Thiết bị này là một quả bóng hình trụ làm bằng polyethylen, nằm trong động mạch chủ, khoảng 2cm, ngay dưới lỗ xuất phát của động mạch dưới đòn trái. Bóng được bơm căng lên trong thì tâm trương làm tăng dòng máu tới động mạch vành và được làm xẹp xuống nhanh trong thì tâm thu, giúp giảm hậu gánh, tăng dòng máu chảy theo động mạch chủ đến các phần xa của cơ thể. Một máy tính kiểm soát hoạt động bơm bóng bằng heli thường được nối với điện tâm đồ hoặc bộ phận nhận cảm áp lực (pressure transducer) ở đầu xa của catheter cho phép làm lệch pha bơm bóng trong thì tâm thu và tâm trương như miêu tả trên đây.
Bóng đối xung động mạch chủ chỉ định với mục đích hỗ trợ tạm thời các tình trạng rối loạn và suy sụp tuần hoàn cho đến khi cơ tim hồi phục hoặc giải quyết được nguyên nhân gây bệnh (như tái thông mạch vành, giải quyết biến cố cơ học…), giảm hậu gánh, giảm tiêu thụ oxy cơ tim đồng thời tăng tưới máu mạch vành để nuôi dưỡng cơ tim. Bóng đối xung động mạch chủ cải thiện chức năng bơm của tim, tăng cung lượng tim thêm 0.5-0.8 L/phút, tăng huyết áp trung bình thêm 30 mmHg mà không tăng nhịp tim.
Đường cong áp lực động mạch chủ khi đặt bóng đối xung động mạch chủ
-Theo dõi sát và diễn giải biến thiên các thông số huyết động để điều chỉnh chế độ bơm cho phù hợp.
- Theo dõi dấu hiệu thiếu máu chi dưới, tình trạng vết chọc động mạch
- Theo dõi tình trạng thông/tắc của bóng
-Theo dõi tình trạng nhiễm trùng tại chỗ và toàn thân.
- Theo dõi công thức máu, chức năng gan thận, bilirubin máu, LDH máu và xét nghiệm đông máu hàng ngày để loại trừ tan máu.
- Những biến chứng liên quan đến kỹ thuật chọc mạch, đẩy bóng và duy trì sau khi đặt bóng đối xung động mạch chủ:
8. Tài liệu tham khảo
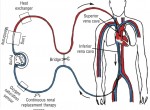
ECMO thường được sử dụng như là một liệu pháp cứu hộ cho bệnh nhân nặng, suy hô hấp có giảm oxy máu dai dẳng mà thất bại với các biện pháp điều trị truyền thống khác.
TRAO ĐỔI OXY QUA MÀNG NGOÀI CƠ THỂ (ECMO)
Extracorporeal Membrane Oxygenation (ECMO)
Tác giả:Matthew Cove, Arthur Boujoukos
Nguồn:
Mechanical Ventilation
John W. Kreit
Oxford University Press, Jan 10, 2013 - Medical - 288 pagesTrong thế kỷ 21, quyển sách về thông khí nhân tạo sẽ không được hoàn thiện nếu không có chương “Trao đổi oxy qua màng ngoài cơ thể” (Extracorporeal Membrane Oxygenation - ECMO). Mặc dù không thường xuyên được sử dụng, và chỉ có ở những trung tâm chuyên khoa, ECMO có khả năng đảm bảo sử trao đổi khí đầy đủ khi thông khí nhân tạo thất bại. Nó là một kỹ thuật hồi sức cấp cứu quan trọng cho hầu hết các bệnh nhân nặng. Vì kết quả điều trị bằng ECMO đang liên tục cải thiện cho nên các bác sĩ hồi sức cấp cứu phải hiểu biết về phương thức hỗ trợ hô hấp này sao cho việc triển khai nhanh chóng và phù hợp có thể được tiến hành ngayChương này sẽ xem xét cơ chế của ECMO, thảo luận làm thế nào để xác định bệnh nhân phù hợp, và cung cấp các thông tin cơ bản về việc làm thế nào để điều trị bệnh nhận đang được ECMO
Lịch sử
Năm 1972, Donald Hill đã báo cáo việc áp dụng ECMO thành công đầu tiên ở một bệnh nhân chấn thương trẻ tuổi có hội chứng suy hô hấp cấp (ARDS) nặng. Sau đó là các báo cáo thành công khác, một nghiên cứu ngẫu nhiên tiến cứu được bảo trợ bởi NIH (NIH-sponsored prospective randomized trial) đã so sánh thông khí nhân tạo truyền thống với thông khí nhân tạo được bổ sung trao đổi oxy qua màng ngoài cơ thể tĩnh mạch-động mạch (veno-arterial ECMO) ở 90 bệnh nhân có ARDS. Được công bố vào năm 1979, chỉ có 4 bệnh nhân (9%) trong mỗi nhóm là sống sót, và ECMO không cho thấy được được là có lợi ích sống còn.Năm 1986, Gattinoni và các đồng nghiệp đã báo cáo rằng việc áp dụng áp dụng kỹ thuật hỗ trợ ngoài cơ thể tĩnh mạch-tĩnh mạch dòng thấp (low-flow veno-venous extracorporeal support) hay còn gọi là đào thải carbon dioxide (CO2) ngoài cơ thể(extracorporeal carbon dioxide removal hoặc ECCO2R) với thông khí nhân tạo tần số thấp đã cho kết quả tỷ lệ sống sót đạt 49% ở nhóm bệnh nhân ARDS nặng. Cải thiện tỷ lệ sống sót ấn tượng này, so với kết quả của nghiên cứu NIH(NIH-sponsored prospective randomized trial), đã khơi dậy mối quan tâm tới kỹ thuật thỗ trợ ngoài cơ thể (extracorporeal support).Lòng nhiệt huyết lại suy yếu một lần nữa vào năm 1994 khi Morris và các đồng nghiệp công bố kết quả nghiên cứu ngẫu nhiên tiến cứu trong việc so sánh ECCO2R và thông khí nhân tạo tần số thấp với thông khí kiểm soát áp lực với tỷ lệ đảo ngược (PC-IRV) ở 40 bệnh nhân có ARDS nặng. Họ không nhận thấy sự khác biệt có ý nghĩa thống kê về tỷ lệ sống sót giữa bệnh nhân được ECCO2R (33%) và bệnh nhân được PC-IRV (43%).Trong thập kỷ sau, nhiều tiến bộ đã được thực hiện trong kỹ thuật ECMO, và nhiều loạt trường hợp đã báo cáo lợi ích của trao đổi oxy qua màng ngoài cơ thể tĩnh mạch-tĩnh mạch dòng cao (high-flow veno-venous ECMO) ở bệnh nhân giảm oxy máu dai dẳng mặc dù đã được hỗ trợ thông khí tối đaNăm 2009, một nghiên cứu đa trung tâm tại Anh đã chọn ngẫu nhiên 180 bệnh nhân có ARDS nặng để điều trị theo phương pháp truyền thống hoặc giới thiệu đến trung tâm chuyên khoa để điều trị bằng trao đổi oxy qua màng ngoài cơ thể tĩnh mạch-tĩnh mạch (veno-venous ECMO hoặc VV-ECMO). Sau 6 tháng, bệnh nhân điều trị tại các trung tâm được giới thiệu tới có nhiều khả năng sống sót mà không có di chứng (63%) hơn những bệnh nhân được điều trị theo phương pháp truyền thống (47%).Cuối cùng, kinh nghiệm trong vụ dịch cúm A/H1N1 năm 2009 – 2010 đã chứng minh rằng VV-ECMO có lợi ích rõ ràng cho những bệnh nhân không đáp ứng với các biện pháp điều trị truyền thống.
Hệ thống tuần hoàn trao đổi oxy qua màng ngoài cơ thể (ECMO Circuit)
Như thấy trong hình 14.1, hệ thống tuần hoàn VV-ECMO bao gồm các ống thông đường vào (access cannulas), ống tráng phủ heparin (heparin-coated tubing), màng trao đổi oxy (oxygenator), bơm máu (blood pump), và bộ trao đổi nhiệt (heat exchanger).Dù theo cách nào thì ECMO vẫn tương tự như thẩm tách máu (hemodialysis). Trong khi thẩm tách (Hình 14.2), máu được rút ra khỏi cơ thể, được bơm qua một màng, và sau đó được trở về hệ thống tuần hoàn cơ thể. Dịch thẩm tách (dialysate) chảy xung quanh màng và tạo lên sự chênh lệch về thẩm thấu và nồng độ, điều này tạo ra sự trao đổi dịch và các chất hòa tan. Tương tự, trong khi ECMO, máu được rút khỏi cơ thể, bơm qua một màng (màng trao đổi oxy) và sau đó trở về tuần hoàn cơ thể. Thay vì dịch thẩm tách, máu được tiếp xúc với khí lưu thông (circulating gas hoặc sweep gas)có một nồng độ phân suất oxy (FO2) được đặt sẵn. Điều này đã tạo ra một sự chênh lệch áp lực riêng phần lớn làm cho O2đi vào và CO2 đi ra khỏi máu. Như thấy trong hình 14.3, màng trao đổi oxy hiện đại được cấu tạo bởi hang ngàn các sợi rỗng cho phép hồng cầu đi vào để tiếp xúc gần với khí lưu thông.
Hình 14.1. Trong khi trao đổi oxy qua màng ngoài cơ thể tĩnh mạch-tĩnh mạch (VV-ECMO), máu thường được rút ra từ tĩnh mạch đùi phải và trở về qua tĩnh mạch cảnh trong phải. Hệ thống tuần hoàn trao đổi oxy qua màng ngoài cơ thể (ECMO circuit) bao gồm các ống thông tiếp cận mạch máu (access cannulas), ống dẫn máu có phủ heparin (heparin-coated tubing), màng trao đổi oxy (oxygenator), bơm máu (blood pump), và bộ trao đổi nhiệt (heat exchanger).
Hình 14.2. Sơ đồ diễn tả hệ thống tuần hoàn thẩm tách máu đơn giản. Sự di chuyển ngược nhau của máu và dịch thẩm tách tạo điều kiện loại bỏ chất hòa tanTốc độ dòng máu ngoài cơ thể trong khi VV-ECMO cao hơn đáng kể trong khi thẩm tách máu. Vì toàn bộ cung lượng tim (CO) được truyền (sử dụng để đẩy máu) qua phổi, do vậy việc trao đổi khí đầy đủ có thể đạt được chỉ bằng cách tạo ra một dòng tương tự qua hệ thống tuần hoàn trao đổi oxy qua màng ngoài cơ thể (ECMO circuit). Điều này được thực hiện bằng việc sử dụng hoặc bơm trục lăn (roller pump) hoặc bơm ly tâm (centrifugal) (Hình 14.4), mặc dù bơm ly tâm thích hợp hơn vì nó gây tan máu ít. Dòng máu ngoài cơ thể lớn có thể gây mất nhiệt, vì vậy bộ trao đổi nhiệt phải được sử dụng để giữ ấm cho máu khi nó đi qua hệ thống tuần hoàn ngoài cơ thể.Như thấy trong hình 14.1, máu thường đi vào hệ tuần hoàn trao đổi oxy qua màng ngoài cơ thể tĩnh mạch-tĩnh mach (VV-ECMO circuit) qua một ống thông (catheter)lớn được đặt qua da vào tĩnh mạch đùi và đi lên tĩnh mạch chủ dưới. Máu trở về tĩnh mạch chủ trên qua một ống thông được luồn vào tĩnh mạch cảnh trong phải. Các ống thông tiên tiến hiện nay cho phép máu được rút ra và trở về hệ tuần hoàn cơ thể qua cùng một vị trí tiếp cận mạch máu (Hình 14.5). Các ống thông này được đặt qua tĩnh mạch cảnh trong phải và tiến vào phần trong gan của tĩnh mạch chủ dưới.Một cấu hình trao đổi oxy qua màng ngoài cơ thể khác là để rút máu từ tĩnh mạch chủ dưới và đưa máu về một động mạch đùi. Cấu hình này được gọi là trao đổi oxy qua màng ngoài cơ thể tĩnh mạch-động mạch (veno-arterial ECMO hoặc VA-ECMO) và nó thường được sử dụng để nhằm hai mục đích trao đổi khí và hỗ trợ huyết động. Thảo luận về VA-ECMO vượt quá tầm của quyển sách này.
Hình 14.3. Sơ đồ diễn tả màng trao đổi oxy (oxygenator) cho thấy sự di chuyển của khí lưu thông (sweep gas) và máu theo hai hướng ngược nhau. Hình ảnh ở bên phải cho thấy mạng sợi rỗng tinh xảo
Hình 14.4. Một bơm trục lăn (roller pump) và một bơm ly tâm (centrifugal pump)
Hình 14.5. Ống thông của kỹ thuật trao đổi oxy qua màng ngoài cơ thể tĩnh mạch-tĩnh mạch trên 2 tĩnh mạch chủ (Bicaval VV-ECMO catheter). Máu được rút ra từ cả hai tĩnh mạch chủ dưới và tĩnh mạch chủ trên và máu trở về tâm nhĩ phải
Biến chứng
Trao đổi oxy qua màng ngoài cơ thể (ECMO) có một vài biến chứng quan trọng và có thể dự báo được. Nhiều biến chứng liên quan tới sự kích hoạt dây truyền đông máu và viêm, nó xảy ra khi máu đi vào và tiếp xúc với tuần hoàn ngoài cơ thể. Màng trao đổi oxy (oxygenator) đặc biệt có vấn đề, vì nó tiếp xúc với máu trên một diện tích rất lớn vật liệu phi sinh học.Thuốc chống đông toàn thân là cần thiết để dự phòng các cục máu đông được hình thành trong màng trao đổi oxy và các cấu tạo khác của tuần hoàn ngoài cơ thể. Không có (hoặc đôi khi có) thuốc chống đông đầy đủ, đông máu có thể làm tắc hệ thống tuần hoàn ngoài cơ thể hoặc thuyên tắc mạch (embolization). Sử dụng hệ thống tuần hoàn ngoài cơ thể được bao phủ heparin, bơm ly tâm, và vật liệu tương thích sinh học hơn đã làm giảm, nhưng không loại bỏ được, các biến chứng này.Kích hoạt dây truyền đông máu còn gây tiêu thụ các yếu tố đông máu và tiểu cầu, điều này có thể dẫn tới bệnh đông máu và giảm tiểu cầu. Đừng ngạt nhiên khi thường thấy chảy máu, đặc biệt khi bệnh nhân được điều trị bằng thuốc chống đông. Các vị trí chảy máu thường thấy bao gồm đường tiêu hóa, nhu mô phổi và đường thở, và tất nhiên cả các vị trí tiếp cận mạch máu. Chảy máu nội sọ ít gặp.ECMO có thể có biến chứng tắc mạch khí, nó có thể là hậu quả của việc mồi(priming) hệ thống tuần hoàn ngoài cơ thể không đúng, hình thành các bong bóng nhỏ trong hệ thống tuần hoàn ngoài cơ thể, hoặc tình cờ cuốn theo khí phòng trong khi đang kết nối hệ thống tuần hoàn ngoài cơ thể. ECMO cũng có thể gây tan máu vì hồng cầu bị đẩy rất nhanh qua các ống thông, ống dẫn, bơm, và màng trao đổi oxy.Cuối cùng, nhiễm trùng bệnh viện, thường gặp nhất là viêm phổi và nhiễm khuẩn huyết, rất phổ biến và đã được báo cáo chiếm khoảng 50 – 60 % bệnh nhân được hỗ trợ ngoài cơ thể. Suy đa phủ tạng chiếm 30 – 40% bệnh nhân và có thể lien quan tới nhiễm trùng hoặc kích hoạt dây truyền đông máu và viêm do hệ thống tuần hoàn trao đổi oxy qua màng ngoài cơ thể (ECMO circuit).
Lựa chọn bệnh nhân
Chỉ định và chống chỉ định với VV-ECMO được liệt kê ở bảng 14.1. ECMO thường được sử dụng như là một liệu pháp cứu hộ cho bệnh nhân nặng, suy hô hấp có giảm oxy máu dai dẳng mà thất bại với các biện pháp điều trị truyền thống khác. Chống chỉ định tương đối bao gồm tuổi trên 65, suy đa phủ tạng, thông khí nhân tạo kéo dài, đang có chẩy máu, và tổn thương thần kinh nặng.
Quy trình điều trị bệnh nhân đang được trao đổi oxy qua màng ngoài cơ thể
Hệ thống tuần hoàn trao đổi oxy qua màng ngoài cơ thể
Ở bệnh nhân đang được ECMO, trao đổi khí chủ yếu được thực hiện trong màng trao đổi oxy (oxygenator) của hệ thống tuần hoàn ngoài cơ thể hơn là ở trong phổi. Ba cài đặt có thể được điều chỉnh dựa vào các phép đo độ bão hòa oxy máu động mạch (SaO2), áp lực riêng phần của CO2 (PaCO2), và áp lực riêng phần của O2 (PaO2): (1) tốc độ dòng khí qua màng trao đổi oxy; (2) nồng độ phân suất oxy (FO2) của khí lưu thông (sweep gas); và (3) tốc độ máu được bơm qua hệ thống tuần hoàn ngoài cơ thểTốc độ dòng khí
Tốc độ khí CO2Â được loại bỏ khỏi máu tĩnh mạch trong hệ thống tuần hoàn ngoài cơ thể tỷ lệ thuận với tốc độ dòng khí qua màng trao đổi oxy. Vì vậy tăng dòng khí lưu thông sẽ làm giảm PaCO2, và giảm dòng khí lưu thông sẽ làm tang PaCO2
| Bảng 14.1. Chỉ định và chống chỉ định với VV_ECMO |
|
| Chỉ định |
Chống chỉ định |
| · ARDS có giảm oxy máu dai dẳng và/hoặc tang carbon oxide o Viêm phổi o Sặc phổi lớn o Đụng dập phổi |
· Tuổi cao/có bệnh lý nặng từ trước · Chống chỉ định sử dụng thuốc chống đông · Suy đa phủ tạng không thể cải thiện với ECMO |
| · Đào thải phổi ghép |
· Tổn thương thần kinh không hồi phục |
| · Tổn thương phổi cấp lien quan tới truyền máu |
· Thông khí nhân tạo > 7 – 10 ngày |
Nồng độ phân áp oxy (FO2)
PaO2 và SaO2thay đổi thuận với FO2 của khí lưu thông (sweep gas), FO2 được đặt sao cho PO2 đạt 100 – 150 mmHg trong máu trở về tuần hoàn cơ thể.Tốc độ máu trong hệ thống tuần hoàn ngoài cơ thể
Một yếu tố quyết định thậm chí quan trọng hơn PaO2Â và SaO2Â là tỷ lệ % của cung lượng tim (CO) đi qua hệ thống tuần hoàn ngoài cơ thể. Nếu dòng máu trong hệ thống tuần hoàn ngoài cơ thể thấp hơn đáng kể cung lượng tim (CO) thì máu trở về đã được oxy hóa sẽ pha trộn với một lượng lớn máu tĩnh mạch của bệnh nhân, dẫn tới oxy hóa máu động mạch không đầy đủ. Dòng máu qua hệ thống tuần hoàn ngoài cơ thể được điều chỉnh bằng việc thay đổi tốc độ (vòng trên phút) của bơm máuThường rất khó khan để duy trì dòng máu trong hệ tuần hoàn ngoài cơ thể được tối ưu. Khi dòng máu không đủ, tăng thể tích lòng mạch và/hoặc thay đổi kích cỡ, số lượng và vị trí của ống thông tiếp cận mạch máu có thể làm cải thiện được hiệu quả và hiệu quả của ECMOHệ thống tuần hoàn trao đổi oxy qua màng ngoài cơ thể cần phải được kiểm tra hàng ngày xem có cục máu đông không, đặc biệt chú ý tới các kết nối ống và màng trao đổi oxy. Để dự phòng sự hình thành cục máu đông, bệnh nhân cần được duy trì heparin truyền tĩnh mạch lien tục với mục tiêu APTT cần đạt 50 – 70 giây. Để giảm thiểu biến chứng chảy máu, số lượng tiểu cầu cần được duy trì trên 80 x 109.
Thông khí nhân tạo
VV_ECMO rất có hiệu quả trong việc loại bỏ CO2Â và duy trì PaO2Â và pH trong giới hạn bình thường. Khi oxy hóa máu đầy đủ, mục tiêu của thông khí nhân tạo là giữ cho phế nang mởÂ (alveolar recruitment)Â mà không gây hư tổn thêm cho phổi tổn thương. Thiết lập thông số thông khí nhân tạo gợi ý được trình bầy trong bảng 14.2. Vt có thể được giảm xuống 200 – 300 ml và tần số giảm xuống 4 – 6 nhịp/phút. PEEP thường được đặt 10 – 15 cmH2O, và FiO2Â thường được đặt ≤ 0,4Thật không may, oxy hóa máu thường không phù hợp bởi vì cung lượng tim vượt quá công suất dòng của hệ thống tuần hoàn ngoài cơ thể. Trong những trường hợp như vậy, FiO2Â và PEEP cao được sử dụng để cố gắng làm cải thiện PaO2và SaO2.
Cai ECMO
Quá trình tách bệnh nhân ra khỏi ECMO nên được bắt đầu khi có bằng chứng cải thiện đáng kể bệnh lý phổi nền của bệnh nhân. Điều này thường được căn cứ vào biểu hiện trên X-quang phổi và sự cải thiện PaO2 và SaO2, và độ đàn hồi của hệ hô hấp. Các thử nghiệm được thực hiện bằng việc tăng FiO2, tần số, và PEEP và tắt khí lưu thông (sweep gas) trong khi vẫn duy trì dòng máu qua hệ thống tuần hoàn trao đổi oxy qua màng ngoài cơ thể. Nếu SaO2 tụt xuống dưới 90%, thì duy trì lại dòng khí lưu thông. Các thử nghiệm được làm lại tối thiểu là hang ngày cho tới khi oxy hóa máu đầy đủ và thông khí nhân tạo được duy trì mà không cần sự hỗ trợ của ECMO
| Bảng 14.2. Cài đặt máy thở |
|
| Phương thức (Mode) |
Kiểm soát hỗ trợ (AC) |
| Kiểu thở (Breath type) |
VC, PRVC |
| Tần số cài đặt (Set Rate) |
4 – 6 lần/phút |
| Vt |
200 – 300 ml |
| PEEP |
10 – 15 cmH2O |
| FiO2 |
0,3 – 0,4 |
Kết luận
ECMO mang tới cho các bác sĩ hồi sức cấp cứu một công cụ quan trọng để có thể hỗ trợ bệnh nhân khi thông khí nhân tạo thất bại. Mặc dù khái niệm còn đơn giản, nhưng việc điều trị những bệnh nhân này đòi hỏi kinh nghiệm và hệ thống hỗ trợ tích cực và vì vậy, ECMO chỉ nên được dùng ở các trung tâm chuyên khoa. Điều quan trọng là tất cả các bác sĩ điều trị bệnh nhân thông khí nhân tạo có thể biết bệnh nhân của họ sẽ có lợi từ ECMO để giới thiệu kịp thời tới một trung tâm ECMO
Đọc thêm
1. Sidebotham D, Mc George A, McGuinness S, et al. Extracorporeal membrane oxygenation for treating severe cardiac and respiratory disease in adults. Part 1: Overview of extracorporeal membrane oxygenation. J Cardiothorac Vasc Anesth 2009; 23:886-8922. Sidebotham D, Mc George A, McGuinness S, et al. Extracorporeal membrane oxygenation for treating severe cardiac and respiratory disease in adults. Part 2: Technical considerations. J Cardiothorac Vasc Anesth 2009; 23:886-8923. Peek GJ, Mugford M, Tiruvoipati R, et al. Efficacy and economic assessment of conventional ventilator support versus extracorporeal membrane oxygenation for severe adult respiratory failure. Lancet 2009; 374: 1351-1363
Trang 1 trong tổng số 18